گزارش جامع درباره ویروس هانتا و شیوع سویه آندس در کشتی «اموی هوندیوس»
در اوایل ماه مه ۲۰۲۶، جهان شاهد رخدادی نادر اما هشداردهنده در حوزه بیماریهای عفونی بود. سازمان جهانی بهداشت (WHO) از شناسایی خوشهای از موارد بیماری شدید ناشی از هانتاویروس در میان مسافران و خدمه کشتی اکتشافی-گردشگری «اموی هوندیوس» خبر داد؛ رخدادی که بار دیگر توجه متخصصان را به خطر بیماریهای مشترک میان انسان و حیوان جلب کرد.
این کشتی هلندی با پرچم هلند، سفر خود را اول آوریل ۲۰۲۶ از شهر اوشوآیا در جنوبیترین نقطه آرژانتین آغاز کرده بود و حدود ۱۴۷ نفر شامل ۸۷ مسافر و ۶۰ خدمه از ۲۳ کشور مختلف در آن حضور داشتند. بر اساس گزارشهای اولیه، منشأ احتمالی آلودگی به سویه «آندس» از هانتاویروسها (Andes virus یا ANDV) مرتبط دانسته شد؛ سویهای که عمدتاً در آرژانتین و شیلی دیده میشود و بهدلیل قابلیت محدود انتقال انسانبهانسان، از سایر هانتاویروسها متمایز است.
تا این لحظه، مقامهای آرژانتینی و چند گزارش رسانهای، یک مسافر هلندی را بهعنوان «مورد شاخص احتمالی» این شیوع معرفی کردهاند؛ فردی که پیش از سوار شدن به کشتی، سفری چندماهه در آرژانتین، شیلی و اروگوئه داشته است. فرضیه اصلی این است که او پیش از آغاز سفر دریایی، در جایی در جنوب آمریکای جنوبی با ویروس تماس پیدا کرده باشد؛ شاید از طریق حضور در محیطهایی که امکان تماس با جوندگان آلوده یا فضولات آنها وجود داشته است. با این حال، این روایت هنوز قطعی نیست. مقامهای بهداشتی آرژانتین در حال بررسی مسیر سفر، ردیابی تماسها و آزمایش نمونههای محیطی و جوندگان هستند. بنابراین در متن علمی دقیقتر است که از تعبیر «مورد شاخص احتمالی» استفاده شود، نه «بیمار صفر قطعی».
تا ۱۲ مه ۲۰۲۶، مقامهای بهداشتی دستکم ۱۱ مورد بیماری را گزارش کردند که ۹ مورد آن تأییدشده و ۲ مورد محتمل بود. در این میان، سه نفر جان خود را از دست دادند؛ نرخ مرگومیر اولیه حدود ۳۸٪ در گزارشهای اولیه (این عدد بر مبنای 8 ابتلای اولیه محاسبه شده است اما با ادامه تحقیقات و تغییر وضعیت ممکن است برآورد نهایی تغییر کند.)
آماری که نرخ مرگومیر موردی بیماری را به حدود ۲۷ درصد میرساند، هرچند این رقم با ادامه بررسیها ممکن است تغییر کند. بیماران دچار «سندرم قلبی-ریوی هانتا» (Hantavirus Cardiopulmonary Syndrome یا HCPS) شده بودند؛ بیماریای که معمولاً با تب، درد عضلانی، سردرد و خستگی آغاز میشود اما میتواند ظرف مدت کوتاهی به تجمع مایع در ریهها، نارسایی شدید تنفسی و شوک قلبی-عروقی منجر شود.
این شیوع بهویژه از آن جهت توجه جهانی را جلب کرد که ویروس آندس تنها هانتاویروس شناختهشدهای است که در شرایط خاص امکان انتقال محدود میان انسانها را دارد؛ هرچند متخصصان تأکید میکنند این انتقال معمولاً نیازمند تماس نزدیک و طولانیمدت با فرد بیمار است و شواهدی مبنی بر انتقال گسترده هوابرد آن وجود ندارد.
کشتی پس از توقفی اضطراری در نزدیکی کیپورد برای تخلیه برخی بیماران، سرانجام به تنریف در جزایر قناری اسپانیا رسید؛ جایی که بخشی از مسافران و خدمه تحت قرنطینه، آزمایش و پایش پزشکی قرار گرفتند. سازمان جهانی بهداشت و مرکز اروپایی پیشگیری و کنترل بیماریها (ECDC) اعلام کردهاند که خطر این شیوع برای جمعیت عمومی در حال حاضر پایین ارزیابی میشود، اما این رویداد بار دیگر نشان داد که بیماریهای زئونوتیک—بیماریهای قابل انتقال از حیوان به انسان—در جهان بهشدت بههمپیوسته امروز همچنان میتوانند به سرعت به مسئلهای بینالمللی تبدیل شوند.
ویروس هانتا و ویژگیهای زیستی آن
هانتاویروسها گروهی از ویروسهای RNA هستند که عمدتاً در میان جوندگان وحشی گردش میکنند و گاهی میتوانند به انسان منتقل شوند. این ویروسها امروزه در ردهبندی جدید ویروسشناسی در خانواده «هانتاویریده» (Hantaviridae) و جنس «اورتوهانتاویروس» (Orthohantavirus) قرار میگیرند؛ هرچند در منابع قدیمیتر اغلب بهعنوان بخشی از خانواده «بونیاویریده» معرفی میشدند. ژنوم این ویروسها از RNA تکرشتهای با قطبیت منفی تشکیل شده است.
«قطبیت منفی» در ویروسهای RNA به این معناست که ماده ژنتیکی ویروس مستقیماً قابل خواندن و استفاده توسط سلول میزبان نیست.
در سلولهای زنده، برای ساخته شدن پروتئینها، معمولاً RNA باید به شکلی باشد که ریبوزومهای سلول بتوانند آن را مستقیماً «بخوانند». به این نوع RNA، «RNA با قطبیت مثبت» گفته میشود. اما RNA هانتاویروس برعکس این حالت است؛ یعنی مانند تصویر معکوس یا نگاتیو یک متن عمل میکند و سلول نمیتواند فوراً آن را ترجمه کند.
به همین دلیل، ویروس باید همراه خود آنزیمی به نام «RNA پلیمراز وابسته به RNA» وارد سلول کند. این آنزیم ابتدا نسخهای مکمل و قابلخواندن از RNA ویروس میسازد و سپس سلول میتواند بر اساس آن پروتئینهای ویروسی را تولید کند. در واقع، ویروس پیش از آغاز تکثیر، مجبور است RNA خود را «ترجمهپذیر» کند.
این ویژگی چند پیامد مهم دارد. نخست اینکه ویروس برای آغاز عفونت به آنزیم اختصاصی خودش وابسته است؛ به همین دلیل ژن مربوط به این پلیمراز در بخش «L» ژنوم هانتاویروس قرار دارد. دوم اینکه فرایند رونویسی و تکثیر RNA در ویروسهای RNA منفی معمولاً خطاپذیرتر از DNA است و همین موضوع میتواند زمینهساز جهش و تنوع ژنتیکی شود.
برای درک سادهتر، میتوان گفت اگر RNA مثبت مانند یک متن عادی قابل خواندن باشد، RNA منفی شبیه نگاتیو فیلم عکاسی است؛ ابتدا باید به تصویر مثبت تبدیل شود تا قابل استفاده باشد.
این ویروس سه بخش اصلی دارد: بخش «L» که دستور ساخت آنزیم پلیمراز ویروسی را حمل میکند، بخش «M» که مسئول تولید گلیکوپروتئینهای سطح ویروس است و بخش «S» که پروتئین نوکلئوکپسید را رمزگذاری میکند. این ساختار چندبخشی به ویروس اجازه میدهد در برخی شرایط دچار «بازآرایی ژنتیکی» یا تبادل قطعات ژنی شود؛ فرایندی که میتواند به ایجاد تنوع ژنتیکی میان سویهها منجر شود.
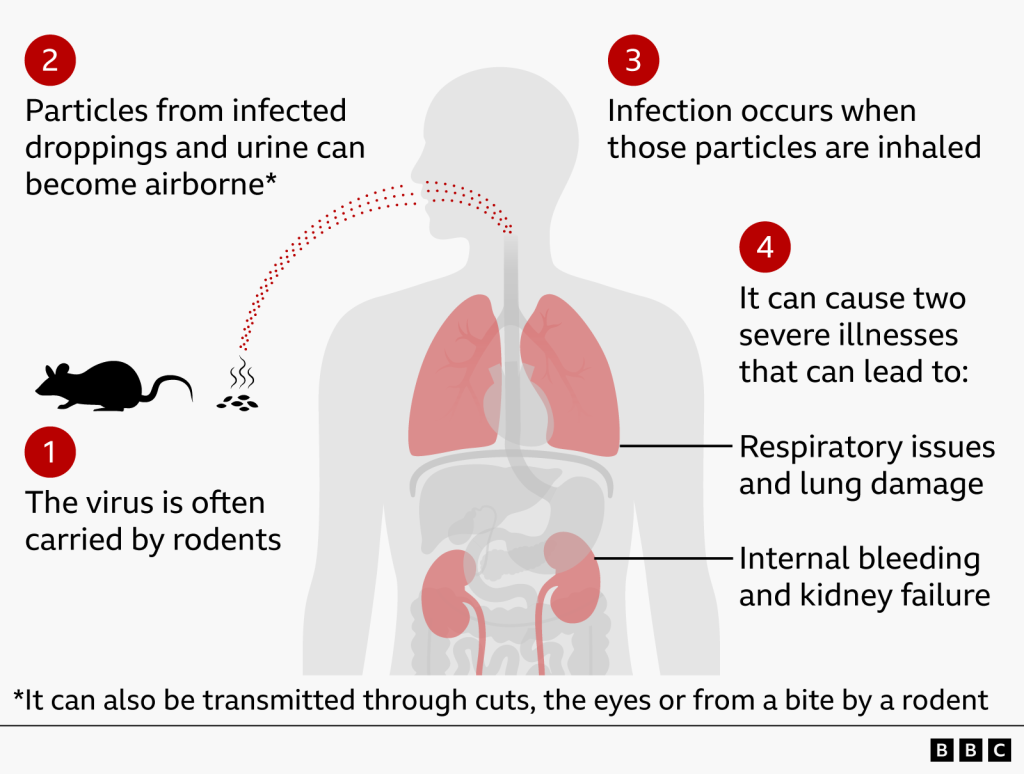
هانتاویروسها معمولاً از طریق تماس با ادرار، مدفوع یا ترشحات جوندگان آلوده به انسان منتقل میشوند. پس از ورود به بدن، این ویروسها میتوانند دو سندرم اصلی ایجاد کنند. در اروپا و آسیا، گونههای مختلف هانتا بیشتر باعث «تب خونریزیدهنده همراه با سندرم کلیوی» میشوند؛ بیماریای که با تب، افت فشار خون و آسیب کلیوی همراه است. اما در قاره آمریکا، هانتاویروسها عمدتاً با «سندرم قلبی-ریوی هانتا» شناخته میشوند؛ بیماریای خطرناک که میتواند به نارسایی شدید تنفسی منجر شود.
سویه «آندس» که عامل اصلی شیوع اخیر در کشتی «اموی هوندیوس» شناخته شده، عمدتاً در آرژانتین و شیلی دیده میشود و میزبان طبیعی آن نوعی جونده به نام «موش برنجی دمدراز» (Oligoryzomys longicaudatus) است. این سویه از آن جهت اهمیت ویژه دارد که تنها هانتاویروس شناختهشدهای است که توان انتقال محدود میان انسانها را نشان داده است.
با این حال، متخصصان تأکید میکنند که این انتقال بهسادگی بیماریهایی مانند کووید-۱۹ یا سرخک رخ نمیدهد. انتقال معمولاً در شرایط تماس نزدیک و طولانیمدت مشاهده شده است؛ برای مثال در میان اعضای خانواده، همخانهها یا کارکنان درمانی که در تماس مستقیم با ترشحات و مایعات بدن بیماران بودهاند. تاکنون شواهد معتبری مبنی بر انتقال گسترده هوابرد این ویروس در محیط عمومی وجود ندارد.
بررسیهای ژنتیکی روی نمونههای مربوط به شیوعهای اخیر نشان میدهد که سویههای درگیر شباهت زیادی با سویههای شناختهشدهای مانند «اپویِن ۱۸-۱۹» و «اپیلینک ۹۶» دارند؛ دو خوشه ویروسی که پیشتر در شیوعهای آرژانتین شناسایی شده بودند. این مطالعات همچنین نشان میدهد که ویروس آندس در مجموع پایداری ژنتیکی نسبتاً بالایی دارد، هرچند مانند بسیاری از ویروسهای RNA همچنان تحت نظارت دقیق دانشمندان قرار دارد تا هرگونه تغییر احتمالی در قدرت بیماریزایی یا الگوی انتقال آن بهسرعت شناسایی شود.
تاریخچه هانتاویروس و شیوعهای مهم گذشته
داستان هانتاویروسها در جهان مدرن از جنگ کره در اوایل دهه ۱۹۵۰ آغاز شد؛ زمانی که هزاران سرباز سازمان ملل دچار تب شدید، خونریزی و نارسایی کلیوی شدند. پژوهشگران بعدها عامل این بیماری را ویروسی شناسایی کردند که نام خود را از رودخانه «هانتان» در کره گرفت؛ منطقهای که نخستین موارد در آن مشاهده شده بود.
برای چند دهه، هانتاویروسها بیشتر بهعنوان بیماریهایی مرتبط با آسیا و اروپا شناخته میشدند، تا اینکه در سال ۱۹۹۳ آمریکا با شیوعی مرموز در منطقه «فور کورنرز» در جنوبغرب ایالات متحده روبهرو شد؛ ناحیهای که مرزهای نیومکزیکو، آریزونا، یوتا و کلرادو به هم میرسند. جوانان سالمی بهطور ناگهانی دچار نارسایی شدید تنفسی میشدند و برخی ظرف چند ساعت جان خود را از دست میدادند.
پژوهشها نشان داد عامل بیماری، سویهای تازه از هانتاویروس است که بعدها «سین نومبر» (Sin Nombre virus) نام گرفت؛ عبارتی اسپانیایی به معنی «بینام». این رویداد نخستین بار توجه گسترده جهان را به «سندرم قلبی-ریوی هانتا» در قاره آمریکا جلب کرد.
«برخلاف برخی بزرگنماییها در رسانهها، این ویروس و شیوع محدود آن روی کشتی هیچ خطر جدی برای تبدیل شدن به یک همهگیری جهانی مشابه کووید-۱۹ ندارد. سازمان بهداشت جهانی خطر جهانی را پایین ارزیابی کرده و متخصصان تأکید دارند که الگوی انتقال این ویروس کاملاً متفاوت از ویروسهای تنفسی به شدت مسری است.»
اما در میان انواع مختلف هانتاویروس، سویه «آندس» جایگاهی ویژه دارد. در سال ۱۹۹۶، در منطقه «ال بولسون» در آرژانتین، پژوهشگران برای نخستین بار شواهد قانعکنندهای از انتقال محدود انسانبهانسان این ویروس پیدا کردند؛ موضوعی که تا آن زمان در مورد هانتاویروسها تقریباً ناشناخته بود.
یکی از مهمترین شیوعهای ثبتشده مربوط به سالهای ۲۰۱۸ تا ۲۰۱۹ در شهر «اپویِن» در استان چوبوت آرژانتین بود. در آن رویداد، دستکم ۳۴ نفر مبتلا شدند و ۱۱ نفر جان خود را از دست دادند؛ یعنی نرخ مرگومیر حدود ۳۲ درصد. بررسیهای اپیدمیولوژیک نشان داد که شیوع احتمالاً با یک انتقال اولیه از جوندگان آغاز شده و سپس از طریق تماسهای نزدیک انسانی گسترش یافته است. حتی حضور در مهمانیها و گردهماییهای خانوادگی نیز در زنجیره انتقال نقش داشت.
پژوهشگران در آن زمان متوجه شدند که برخی بیماران نقش مهمتری در انتقال بیماری داشتهاند؛ پدیدهای که در اپیدمیولوژی به آن «ابرانتقالدهنده» یا superspreader گفته میشود. این افراد معمولاً بار ویروسی بالاتری داشتند؛ یعنی مقدار بیشتری ویروس در بدن آنها وجود داشت و بیماری در آنها شدیدتر بود. مطالعات همچنین نشان داد که میزان آسیب کبدی و شدت پاسخ ایمنی در این بیماران بیشتر بوده است.
برآوردها نشان میداد عدد بازتولید پایه یا R0 در آغاز شیوع اپویِن حدود ۲٫۱ بوده؛ یعنی هر بیمار میتوانست بهطور متوسط بیش از دو نفر دیگر را آلوده کند. اما پس از قرنطینه، ردیابی تماسها و محدودیتهای بهداشتی، این عدد به کمتر از یک کاهش یافت و زنجیره انتقال متوقف شد.
هانتاویروس چگونه به بدن آسیب میزند؟
یکی از ویژگیهای عجیب هانتاویروسها این است که معمولاً سلولها را مستقیماً نابود نمیکنند. ویروس عمدتاً سلولهای اندوتلیال را هدف میگیرد؛ سلولهایی که دیواره داخلی رگهای خونی را میپوشانند و نقش مهمی در کنترل عبور مایعات از مویرگها دارند.
اما آسیب اصلی بیشتر ناشی از واکنش شدید سیستم ایمنی بدن است تا خود ویروس. هنگامی که بدن حضور ویروس را تشخیص میدهد، سیستم ایمنی بهسرعت فعال میشود و حجم زیادی از مولکولهای التهابی موسوم به «سیتوکین» آزاد میکند؛ موادی مانند TNF-α، اینترلوکین-۶ و اینترفرون گاما.
در برخی بیماران، این پاسخ ایمنی از کنترل خارج میشود و چیزی شکل میگیرد که دانشمندان آن را «طوفان سیتوکینی» مینامند. در این وضعیت، دیواره مویرگها بیشازحد نفوذپذیر میشود و مایع از رگها به درون بافتها نشت میکند. در ریهها، این فرایند میتواند باعث تجمع سریع مایع، ادم ریوی و نارسایی تنفسی شود؛ حتی در حالی که قلب در ابتدا سالم است.
همزمان، افت شدید حجم مایع درون رگها میتواند به شوک هیپوولمیک منجر شود؛ وضعیتی که در آن فشار خون سقوط میکند و اندامهای حیاتی با کمبود اکسیژن روبهرو میشوند.
مطالعات نشان میدهد هرچه بار ویروسی بیمار بیشتر باشد، خطر بیماری شدیدتر و احتمال انتقال ویروس نیز بیشتر میشود. در مدلهای حیوانی—بهویژه در همسترها که یکی از مهمترین مدلهای آزمایشگاهی برای مطالعه ویروس آندس هستند—پژوهشگران مشاهده کردهاند که سویه آندس التهاب شدیدتر و آسیب عروقی گستردهتری ایجاد میکند، در حالی که برخی سویههای غیرپاتوژن هانتاویروس چنین واکنش شدیدی را برنمیانگیزند.
همین ویژگیهاست که هانتاویروس را به بیماریای خطرناک اما از نظر زیستشناسی بسیار جالب برای ویروسشناسان و متخصصان ایمنیشناسی تبدیل کرده است.
آیا هانتاویروس میتواند به یک پاندمی جهانی تبدیل شود؟
هر بار که خبر شیوع یک ویروس جدید منتشر میشود، یکی از نخستین پرسشها این است: آیا این میتواند آغاز پاندمی بعدی باشد؟
در مورد هانتاویروسها، پاسخ فعلی دانشمندان محتاطانه اما نسبتاً آرامشبخش است. برخلاف ویروسهایی مانند آنفلوانزا یا کروناویروسها، هانتاویروسها بهطور کلی توان انتقال بالایی میان انسانها ندارند و بیشتر موارد بیماری همچنان نتیجه تماس مستقیم یا غیرمستقیم با جوندگان آلوده است.
البته ویروسها موجوداتی ثابت نیستند. هانتاویروسها نیز مانند بسیاری از ویروسهای RNA در طول زمان دچار جهش میشوند. علاوه بر جهشهای معمول، ساختار چندبخشی ژنوم آنها امکان نوعی «بازآرایی ژنتیکی» را فراهم میکند؛ فرایندی که در آن بخشهایی از ژنوم میان دو سویه مختلف جابهجا میشود و میتواند ویژگیهای تازهای ایجاد کند.
دانشمندان نگراناند که فشارهای محیطی و انتخاب طبیعی—برای مثال گردش طولانی ویروس در میان میزبانهای مختلف—در آینده بتواند بر شدت بیماریزایی یا الگوی انتقال برخی سویهها اثر بگذارد. با این حال، تاکنون هیچ شواهد معتبری وجود ندارد که نشان دهد سویه آندس در شیوع ۲۰۲۶ به شکل هوابرد گسترده یا بسیار مسری تکامل یافته باشد.
با وجود این، متخصصان بر اهمیت «پایش ژنومی» تأکید میکنند؛ یعنی توالییابی مداوم ویروس برای شناسایی سریع هرگونه تغییر ژنتیکی مهم. تجربه پاندمی کووید-۱۹ نشان داد که نظارت ژنتیکی سریع میتواند در تشخیص سویههای جدید و ارزیابی خطر آنها نقشی حیاتی داشته باشد.
چرا کشتیها و محیطهای بسته حساساند؟
هرچند توان انتقال هانتاویروس محدود است، اما محیطهای بسته میتوانند شرایط را تغییر دهند. کشتیها، خوابگاهها، پادگانها یا خانههایی که افراد برای مدت طولانی در تماس نزدیک با یکدیگر هستند، میتوانند احتمال انتقال را افزایش دهند.
در چنین محیطهایی، تماس مداوم با ترشحات تنفسی، سرفه، مایعات بدن یا مراقبت نزدیک از بیماران ممکن است شانس انتقال را بیشتر کند. به همین دلیل، مقامهای بهداشتی در شیوع اخیر بهسرعت سراغ قرنطینه، ردیابی تماسها و نظارت پزشکی رفتند.
کارشناسان میگویند یکی از دلایل اصلی کنترل سریع این شیوع، واکنش نسبتاً سریع سامانههای بهداشتی و تجربه بهدستآمده از اپیدمیهای اخیر جهانی بوده است.
سطح واقعی خطر چقدر است؟
سازمان جهانی بهداشت و مرکز اروپایی پیشگیری و کنترل بیماریها در ارزیابیهای اولیه خود اعلام کردهاند که خطر این شیوع برای جمعیت عمومی پایین است، هرچند برای افراد حاضر در کشتی یا تماسهای نزدیک بیماران، خطر در سطح متوسط ارزیابی میشود.
این ارزیابی بر چند عامل استوار است: نبود شواهد انتقال گسترده در جامعه، محدود بودن زنجیرههای انتقال، نبود موارد ثانویه گسترده در خارج از کشتی و کنترل سریع بیماران و تماسهای نزدیک.
با این حال، متخصصان هشدار میدهند که این رویداد نباید صرفاً بهعنوان یک حادثه محلی دیده شود. در سالهای اخیر، موارد هانتاویروس در برخی مناطق آمریکای جنوبی افزایش یافته و همزمان، سفرهای جهانی و جابهجایی سریع انسانها میتواند بیماریهای منطقهای را ظرف چند روز به مسئلهای بینالمللی تبدیل کند.
به همین دلیل، بسیاری از اپیدمیولوژیستها شیوع «اموی هوندیوس» را نه نشانه آغاز یک پاندمی جهانی، بلکه هشداری درباره آسیب پذیری بودن جهان مدرن در برابر بیماریهای زئونوتیک میدانند؛ بیماریهایی که در دنیای بههمپیوسته امروز میتوانند از یک منطقه دورافتاده به سرعت وارد شبکه جهانی سفر و تجارت شوند.
چرا درمان هانتاویروس دشوار است؟
برخلاف بسیاری از عفونتهای باکتریایی، برای هانتاویروس هنوز درمان اختصاصی و قطعی وجود ندارد. پزشکان در عمل بیشتر تلاش میکنند بدن بیمار را تا زمانی که سیستم ایمنی بتواند ویروس را کنترل کند، زنده و پایدار نگه دارند.
در مراحل اولیه، تشخیص سریع بیماری اهمیت حیاتی دارد، زیرا وضعیت بیماران ممکن است در مدت کوتاهی بهشدت وخیم شود. آزمایشهای مولکولی مانند PCR و توالییابی ژنتیکی میتوانند در شناسایی سریع ویروس کمک کنند.
در موارد شدید، بیماران به اکسیژن، دستگاه تنفس مصنوعی و مراقبتهای ویژه نیاز پیدا میکنند. در برخی موارد بحرانی، از دستگاه ECMO نیز استفاده میشود؛ فناوریای که بهطور موقت وظیفه ریه و گاهی قلب را بر عهده میگیرد تا بدن فرصت بازیابی پیدا کند.
برخی داروهای ضدویروسی مانند «ریباویرین» در برخی انواع هانتاویروس—بهویژه گونههای مرتبط با آسیب کلیوی در آسیا—اثراتی نشان دادهاند، اما نقش آنها در سندرم قلبی-ریوی هانتا هنوز محدود و بحثبرانگیز است.
جستوجو برای واکسن
با وجود دههها تحقیق، هنوز واکسن تأییدشده جهانی برای هانتاویروسها وجود ندارد. یکی از دلایل اصلی این موضوع، پراکندگی جغرافیایی محدود بیماری و تعداد نسبتاً کم موارد در مقایسه با بیماریهایی مانند آنفلوانزا یا کووید-۱۹ است؛ مسئلهای که سرمایهگذاری صنعتی گسترده را دشوار کرده است.
برخی واکسنهای غیرفعال در آسیا برای گونههای خاص هانتاویروس استفاده شدهاند، اما میزان اثربخشی آنها متوسط ارزیابی میشود و استفاده جهانی پیدا نکردهاند.
در سالهای اخیر، پژوهشگران به سراغ فناوریهای جدیدتر رفتهاند. از جمله امیدبخشترین پروژهها میتوان به واکسنهای DNA علیه سویه آندس اشاره کرد که در مطالعات اولیه توانستهاند در بخشی از داوطلبان پاسخ ایمنی قابلتوجهی ایجاد کنند. پژوهش درباره آنتیبادیهای مونوکلونال نیز ادامه دارد؛ مولکولهایی آزمایشگاهی که میتوانند مستقیماً ویروس را هدف قرار دهند.
با این حال، بیشتر این فناوریها هنوز در مراحل آزمایشی هستند و احتمالاً سالها تا تولید گسترده فاصله دارند. بسیاری از متخصصان معتقدند تجربه پاندمی کووید-۱۹ شاید در آینده روند توسعه واکسن برای بیماریهای نوظهور زئونوتیک مانند هانتاویروس را سریعتر کند، اما در حال حاضر پیشگیری و تشخیص زودهنگام همچنان مهمترین ابزار مقابله با این بیماری باقی مانده است.
درسهایی فراتر از یک کشتی: چرا جهان به «دفاع پاندمیک» نیاز دارد؟
شیوع ویروس آندس در کشتی اموی هوندیوس اگرچه در نهایت به مرحله مهار رسیده است، اما یادآور واقعیتی مهم بود: جهان همچنان در برابر بیماریهای نوظهور آسیبپذیر است. بسیاری از متخصصان بیماریهای عفونی سالهاست هشدار میدهند که مسئله این نیست که «آیا» پاندمی دیگری رخ خواهد داد یا نه؛ بلکه سؤال اصلی این است که «چه زمانی» رخ خواهد داد.
بخش بزرگی از بیماریهای نوظهور، از جمله هانتاویروسها، منشأ zoonotic دارند؛ یعنی از حیوانات به انسان منتقل میشوند. تغییرات اقلیمی، تخریب زیستگاههای طبیعی، گسترش شهرنشینی، تجارت حیاتوحش و افزایش سفرهای بینالمللی باعث شدهاند تماس میان انسان و مخازن طبیعی ویروسها بیشتر از گذشته شود. در چنین جهانی، حتی یک عفونت محدود در منطقهای دورافتاده میتواند طی چند روز به چندین کشور برسد.
هزینه جنگ بیشتر است یا پیشگیری؟
یکی از نکات بحثبرانگیز در حوزه سلامت جهانی، شکاف عظیم میان هزینههای نظامی و سرمایهگذاری برای آمادگی در برابر پاندمیهاست.
برنامههایی مانند CEPI (ائتلاف نوآوری آمادگی برای همهگیریها)، سامانههای نظارتی سازمان جهانی بهداشت و پروژههای جهانی ردیابی ژنومی، در مجموع تنها چند میلیارد دلار بودجه سالانه دریافت میکنند. این در حالی است که هزینه نظامی جهان در سالهای ۲۰۲۴ و ۲۰۲۵ از مرز ۲٫۷ تریلیون دلار عبور کرده و برخی برآوردها پیشبینی میکنند این رقم تا دهه آینده حتی به بیش از ۴ تا ۶ تریلیون دلار در سال برسد.
برای مقایسه، هزینه توسعه یا نگهداری برخی سامانههای پیشرفته نظامی میتواند با بودجه سالانه بخشی از برنامههای بهداشت جهانی برابری کند. در حالی که تجربه کووید-۱۹ نشان داد یک پاندمی میتواند نهتنها میلیونها قربانی بگیرد، بلکه دهها تریلیون دلار به اقتصاد جهانی آسیب وارد کند.
بسیاری از متخصصان معتقدند سرمایهگذاری در حوزههایی مانند: نظارت ژنومی ویروسها، شبکههای هشدار سریع، توسعه پلتفرمهای واکسن، ظرفیت مراقبتهای ویژه، و رویکرد «One Health» که سلامت انسان، حیوان و محیط زیست را بههمپیوسته میبیند، میتواند با هزینهای بسیار کمتر، از بحرانهای بسیار بزرگتر جلوگیری کند.
جهان چقدر آماده است؟
پس از کووید-۱۹، بسیاری از کشورها وعده دادند که آمادگی جهانی در برابر بیماریهای نوظهور را تقویت کنند، اما بخش مهمی از آن وعدهها هنوز عملی نشده است. کارشناسان بهداشت جهانی بارها هشدار دادهاند که بسیاری از سیستمهای مراقبت و پایش بیماری همچنان کمبود بودجه، نیروی انسانی و هماهنگی بینالمللی دارند.
برخی پیشنهاد میکنند جهان باید سالانه دستکم ۱۰ تا ۲۰ میلیارد دلار بهطور پایدار صرف آمادگی پاندمیک کند؛ رقمی که در مقیاس اقتصاد جهانی و بودجههای نظامی، نسبتاً کوچک محسوب میشود، اما میتواند از خسارتهای انسانی و اقتصادی بسیار بزرگ جلوگیری کند.
شیوع آندس در کشتی اموی هوندیوس احتمالاً به یک پاندمی جهانی تبدیل نخواهد شد، اما ارزش آن را دارد که بهعنوان یک هشدار جدی دیده شود. این رویداد نشان داد که حتی ویروسهایی نسبتاً ناشناخته نیز میتوانند در جهانی بهشدت متصل، به سرعت توجه بینالمللی را جلب کنند.
تجربه هانتاویروس بار دیگر این واقعیت را یادآوری میکند که انسان بخشی از یک اکوسیستم پیچیده است؛ اکوسیستمی که سلامت انسان، حیوانات و محیط زیست در آن به هم گره خوردهاند. در چنین جهانی، سرمایهگذاری در علم، همکاری بینالمللی و نظامهای پیشگیری، نه یک هزینه اضافی، بلکه بخشی از امنیت واقعی جوامع انسانی است.





