پژوهشگران کاتالونیا موفق شدند اندامکهای کلیهٔ انسان را با کلیهٔ خوک ترکیب و دوباره در بدن پیوند بزنند
پژوهشگران مؤسسه مهندسی زیستی کاتالونیا (IBEC) با همکاری مؤسسه تحقیقات زیستپزشکی آکرونیا (INIBIC) و گروههای بینالمللی دیگر، فناوری نوینی توسعه دادهاند که امکان تولید انبوه اندامکهای کلیهٔ انسانی را فراهم میکند.
در این روش، اندامکهای ساختهشده از سلولهای بنیادی انسان با کلیههای خوک در خارج از بدن ترکیب شده و سپس به همان حیوان بازگردانده شدند تا میزان زندهمانی و عملکردشان بررسی شود.
نتایج این پژوهش که در مجله Nature Biomedical Engineering منتشر شده، گامی مهم در مسیر پزشکی بازساختی و درمانهای شخصیسازیشده است.
به گفتهٔ دانشمندان، این فناوری میتواند در آینده راه را برای کاربرد اندامکهای انسانی در پیوند و درمان نارسایی کلیه هموار کند.
از رؤیای اندام مصنوعی تا واقعیت مهندسیشده
سرپرستی این پروژه را دکتر «نوریـا مونسرات» برعهده داشت — کسی که سالها در IBEC بر روی پزشکی بازساختی و زیستمهندسی اندامها کار کرده است و اکنون به عنوان وزیر پژوهش و دانشگاههای دولت کاتالونیا فعالیت میکند.
او و تیمش پس از بیش از ده سال پژوهش مداوم، برای نخستین بار توانستند اندامکهای کلیهٔ انسان را با کلیهٔ زندهٔ خوک ترکیب کنند و عملکرد آنها را در دستگاههای «پرفیوژن نرموترمیک» مورد بررسی قرار دهند.
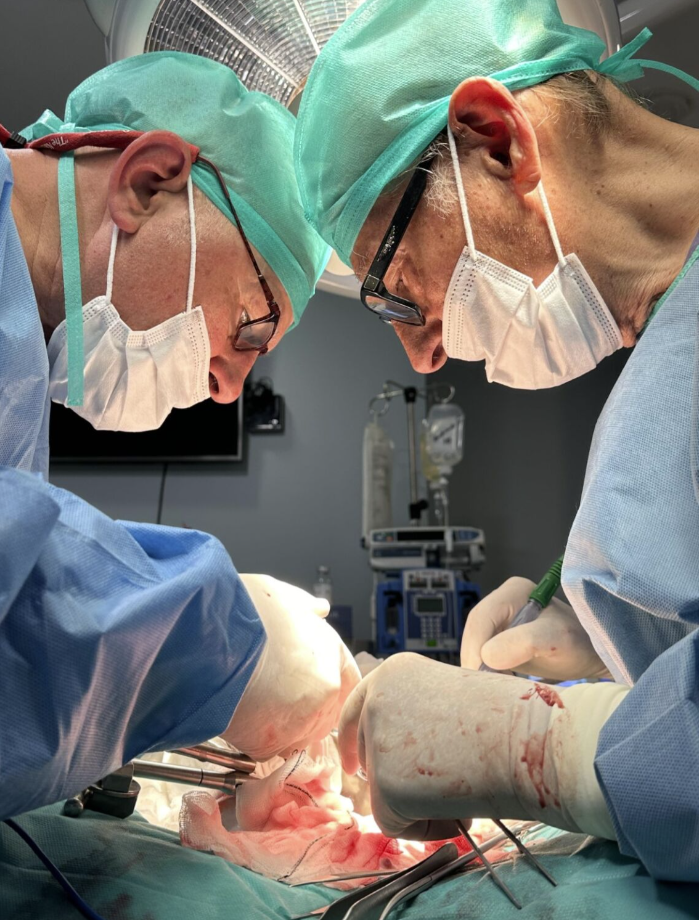
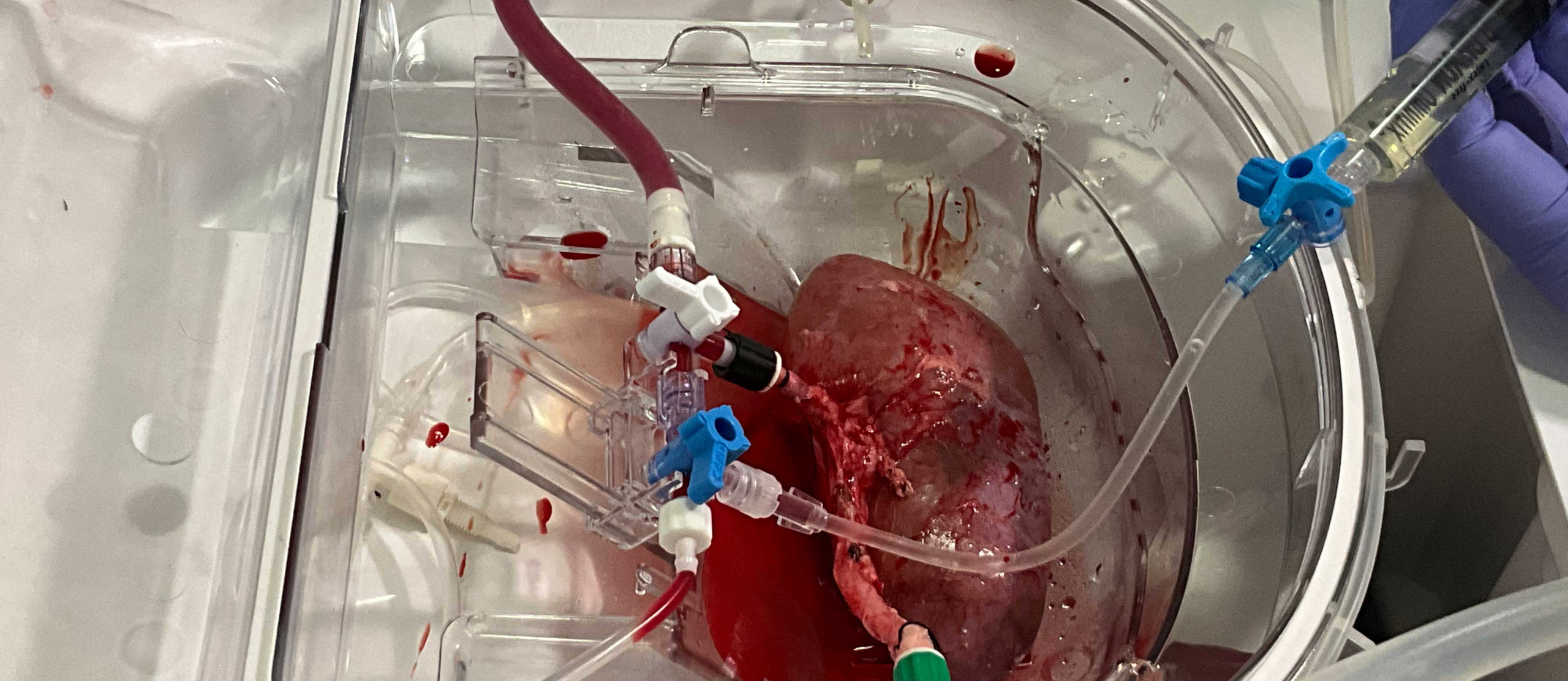
این دستگاهها که در اتاقهای عمل برای حفظ زندهمانی و اکسیژنرسانی اندامها پیش از پیوند استفاده میشوند، به پژوهشگران اجازه داد تا در شرایط کنترلشده، عملکرد اندامکهای انسانی را درون کلیهٔ خوک مشاهده کنند.
دکتر مونسرات توضیح میدهد:
«ترکیب فناوری اندامکها با سامانههای پرفیوژن خارجبدنی، امکان مداخلات سلولی را در شرایط کاملاً کنترلشده فراهم میکند. هدف بلندمدت ما بازسازی یا ترمیم اندام پیش از پیوند است — کاری که میتواند زمان انتظار بیماران را کاهش داده و تعداد اندامهای قابلپیوند را افزایش دهد.»
اندامک کلیه چیست؟
اندامکها (organoids) ساختارهای سهبعدی کوچکی هستند — تنها چند صد میکرومتر قطر دارند — که از سلولهای بنیادی انسان در محیط آزمایشگاه پرورش مییابند.
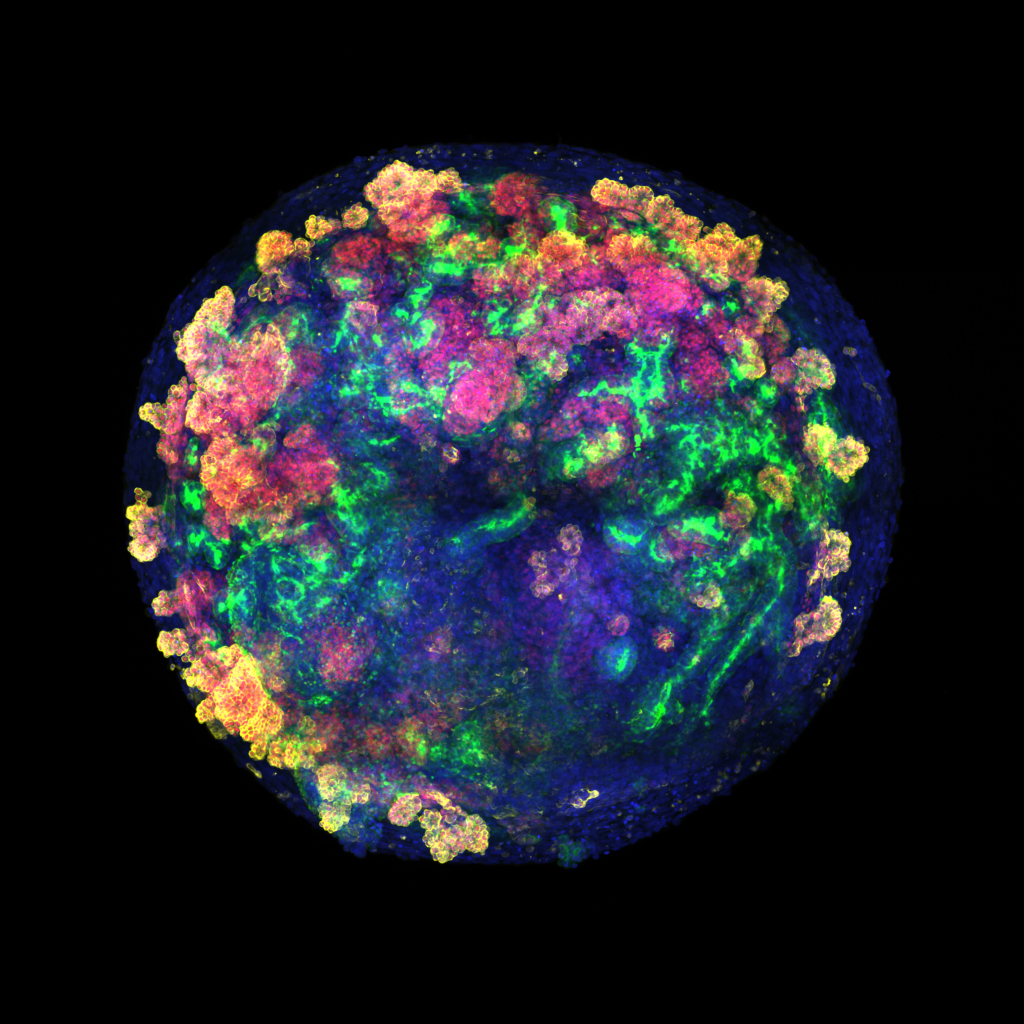
سلولها با استفاده از روش ایمونوفلورسانس به رنگهای مختلف برچسبگذاری شدهاند تا اجزای ویژهای شناسایی شوند:
LTL (سبز: لولههای کلیوی)، WT1 (قرمز: پودوسیتها)، PODXL (زرد: پودوسیتها) و DAPI (آبی: هستهٔ سلولها).
این تصویر سازمانیافتگی انواع مختلف سلولها را در درون اندامک کلیه نشان میدهد.
Credit: Institute for Bioengineering of Catalonia (IBEC)
هرچند اندام کامل محسوب نمیشوند، اما بسیاری از ساختارها و عملکردهای حیاتی کلیهٔ واقعی را بازآفرینی میکنند.
به کمک این ویژگی، اندامکها به ابزاری کلیدی در پژوهشهای پزشکی تبدیل شدهاند:
- مطالعهٔ رشد و تکوین اندامها،
- آزمایش داروهای جدید،
- و اکنون، تلاش برای ترمیم بافتهای آسیبدیده و بهبود اندامهای آمادهٔ پیوند.
تولید انبوه با دقت سلولی
یکی از دستاوردهای بزرگ این پژوهش، توسعهٔ روشی برای تولید هزاران اندامک کلیه در شرایط استاندارد و کنترلشده است.
پژوهشگران با ترکیب فناوری ریزتجمع سلولی (microaggregation) و مهندسی ژنتیک، توانستند فرایند تولید را سیستماتیک و قابل تکرار کنند.

این دستگاه امکان زنده و اکسیژندار نگه داشتن کلیه را در خارج از بدن (ex vivo) فراهم میکند.
در تصویر، لحظهٔ تزریق اندامکهای کلیهٔ انسانی به درون کلیهٔ خوک دیده میشود.
Credit: Institute for Bioengineering of Catalonia (IBEC)
دکتر «النا گارِتا»، پژوهشگر ارشد گروه بازتولید اندام در IBEC و نویسندهٔ اول مقاله، میگوید:
«یکی از چالشهای بزرگ در استفادهٔ پزشکی از اندامکها، تولید آنها بهصورت انبوه، یکنواخت و مقرونبهصرفه بود.
اکنون میتوانیم در مدت کوتاه، هزاران اندامک کلیه با دقت بالا و بدون نیاز به اجزای پیچیده تولید کنیم. این روش دریچهای بهسوی غربالگری دارویی و مطالعهٔ بیماریهای کلیوی میگشاید.»
پیوند در کلیهٔ خوک؛ آزمایش در مقیاس زیستی
در گام بعد، پژوهشگران اندامکهای انسانی را با کلیههای خوک ترکیب کردند — ابتدا در خارج از بدن (ex vivo) و سپس در همان حیوان (in vivo).
مدل خوک به دلیل شباهت فیزیولوژیک بالایش با انسان، یکی از بهترین مدلهای آزمایشی در تحقیقات پیوند محسوب میشود.
در این آزمایشها، پس از ۲۴ و ۴۸ ساعت از پیوند، اندامکهای انسانی همچنان زنده، فعال و در بافت کلیهٔ خوک یکپارچه بودند.
هیچ نشانهای از التهاب یا واکنش ایمنی شدید مشاهده نشد، و عملکرد کلیه نیز طبیعی باقی ماند.
دکتر «گارِتا» توضیح میدهد که استفاده از دستگاههای پرفیوژن نهتنها اکسیژنرسانی اندام را تضمین میکند، بلکه امکان اندازهگیری پارامترهای فیزیولوژیک در زمان واقعی را نیز میدهد.
به این ترتیب، هرگونه نشانهٔ رد پیوند یا آسیب بافتی بلافاصله قابل تشخیص است.
چرا این پژوهش اهمیت دارد؟
پیشرفت تازه میتواند پایهگذار مدلی بالینی باشد که در آن اندامهای پیوندی پیش از قرار گرفتن در بدن بیمار، در محیط آزمایشگاهی بازسازی یا ترمیم شوند.
در چنین سناریویی، اندام اهدایی میتواند با سلولهای بنیادی خود بیمار بازسازی شود تا خطر رد پیوند کاهش یابد.
به گفتهٔ دکتر مونسرات، این فناوری در آینده ممکن است زمان انتظار بیماران دچار نارسایی کلیه را بهطور چشمگیری کاهش دهد.
امروز میلیونها نفر در سراسر جهان در صف پیوند کلیه هستند — اما تنها بخش کوچکی از آنها به اندام سازگار دست مییابند.
فناوری جدید میتواند با ترمیم اندامهای مرزی (که در حالت عادی غیرقابل استفادهاند) یا بهبود اندامهای موجود با سلولهای انسانی، ظرفیت پیوند را گسترش دهد.
همکاری جهانی در خدمت علم
این پروژه نمونهای از همکاری بینالمللی در بالاترین سطح پژوهش زیستپزشکی است.
در کنار IBEC و INIBIC، مؤسسات متعددی از اروپا، چین و ایالات متحده در آن مشارکت داشتهاند، از جمله:
CIBER-BBN، سازمان ملی پیوند اسپانیا (ONT)، دانشگاه بارسلونا، مؤسسه تحقیقات ناوارا، دانشگاه کالیفرنیا، دانشگاه لِوِن، و شرکت فناوری پزشکی EBERS که دستگاههای پرفیوژن را توسعه داده است.
دکتر «النا گارِتا» علاوه بر پژوهش، استاد زیستشناسی سلولی در دانشگاه بارسلونا است و نقش کلیدی در طراحی روش تولید انبوه اندامکها داشته است.
چشمانداز آینده: بازسازی اندام پیش از پیوند
به گفتهٔ نویسندگان، این پژوهش راه را برای آیندهای میگشاید که در آن، اندامهای پیوندی پیش از استفاده، تحت «درمان بازسازی» قرار میگیرند.
به بیان دیگر، پزشکی آینده میتواند پیش از آنکه اندامی به بدن بیمار منتقل شود، نقصهای آن را با سلولهای بنیادی اصلاح کند.

دکتر مونسرات تأکید میکند:
«هدف ما دستیابی به فناوریای است که بتوان با آن اندامی را که قرار است پیوند زده شود، از پیش ترمیم کرد. این مفهوم میتواند تعریف پزشکی بازساختی را دگرگون کند.»
گامی بهسوی پزشکی شخصیسازیشده
در چشمانداز گستردهتر، اندامکهای انسانی میتوانند به ابزارهای کلیدی برای پزشکی فردمحور بدل شوند — یعنی درمانهایی که از سلولهای خود بیمار برای بازسازی بافتهای آسیبدیده استفاده میکنند.
این فناوری همچنین میتواند فرآیند توسعهٔ داروها را دگرگون کند:
به جای آزمایشهای حیوانی پرهزینه و پرخطر، هزاران اندامک انسانی در محیط کنترلشده قابل استفادهاند تا اثر داروها در سطح سلولی و مولکولی بررسی شود.
پژوهش منتشرشده در Nature Biomedical Engineering نهفقط یک دستاورد فناورانه، بلکه اثباتی از بلوغ مهندسی زیستی مدرن است — تلاشی که مرز میان زیستشناسی و فناوری را کمرنگ میکند.
به گفتهٔ پژوهشگران، مسیر پیشرو هنوز طولانی است: چالشهای اخلاقی، ایمنی بالینی و مقرراتی باید حل شوند.
اما چشمانداز نهایی روشن است: روزی اندامهای انسانی ساختهشده از سلولهای خود بیمار، در اتاقهای عمل آمادهٔ پیوند خواهند بود.
در جهانی که کمبود اندامهای پیوندی جان میلیونها نفر را تهدید میکند،
این دستاورد، گامی واقعی بهسوی پزشکیای است که در آن انسان، خالق درمانِ خویش میشود.



