باکتریها و مکانیزم دفاعی ویروسی که به بیماری خودایمنی انسان مرتبط است
محققان موفق شده اند از ارتباط شگفتانگیزی بین یک مکانیزم دفاعی در باکتریها و بیماریهای خودایمنی در انسان برمیدارد. این کشف، که توسط تیمی از دانشمندان در دانشگاه کالیفرنیا، سندیگو انجام شده و در مجلهی Nature منتشر شده، نشان میدهد که سیستمی که باکتریها برای محافظت از خود در برابر ویروسها استفاده میکنند، ممکن است نقشی غیرمنتظره در ایجاد بیماریهایی مانند لوپوس در انسان داشته باشد. این یافته نهتنها درک ما از میکروبها را عمیقتر میکند، بلکه میتواند راه را برای درمانهای جدید هموار کند.
مکانیزم دفاعی باکتریها: سپری در برابر ویروسها
باکتریها، این موجودات میکروسکوپی که در همهجا از خاک و آب گرفته تا بدن ما زندگی میکنند، دائماً در معرض حملهی ویروسهایی به نام باکتریوفاژها (فاژها) هستند. این ویروسها به باکتریها حمله میکنند، ژنهای خود را وارد آنها میکنند و از منابع باکتری برای تکثیر استفاده میکنند. برای دفاع، برخی باکتریها سیستمی به نام CRISPR-Cas توسعه دادهاند. این سیستم مانند یک قیچی ژنتیکی عمل میکند: بخشی از DNA ویروس را برش میدهد و آن را بهعنوان «خاطره» ذخیره میکند تا در حملات بعدی سریعتر واکنش نشان دهد.
شما شاید با ساختار کریسپر به خاطر مطالب متعددی که درباره ماشین CRISPR-Cas9 در سالهای اخیر منتشر و حتی منجر به اهدای جایزه نوبل به کاشفان آن شد آشنا باشید. در غیر این صورت درباره این ماشین مولکولی می توانید این مقالههای پیشین من را مطالعه کنید:
در این مطالعه اما، پژوهشگران روی نوع خاصی از سیستم CRISPR به نام Cas10 تمرکز کردند. این سیستم در باکتریهایی مثل Corynebacterium diphtheriae (عامل بیماری دیفتری) یافت میشود. برخلاف CRISPRهای معمولی که فقط DNA ویروس را هدف قرار میدهند، Cas10 توانایی تولید مولکولهای سیگنالدهندهای به نام cA4 را دارد. این مولکولها به باکتری کمک میکنند تا پاسخ دفاعی گستردهتری علیه ویروسها ایجاد کند، مثل یک زنگ خطر که کل سلول را آمادهی نبرد میکند.
ارتباط با انسان: از باکتری تا بیماری خودایمنی
اما این داستان وقتی جالبتر میشود که به انسانها میرسیم. دانشمندان دریافتند که مولکول cA4، که در باکتریها نقش دفاعی دارد، در بدن انسان هم میتواند اثر بگذارد—اما نه به شکل مثبت. در انسان، این مولکول به سیستمی به نام STING (مخفف Stimulator of Interferon Genes) متصل میشود STING بخشی از سیستم ایمنی ذاتی ماست که معمولاً ویروسها را شناسایی میکند و پاسخ التهابی ایجاد میکند. وقتی cA4 به STING متصل میشود، این سیستم بیشازحد فعال میشود و التهابی غیرضروری به راه میاندازد.
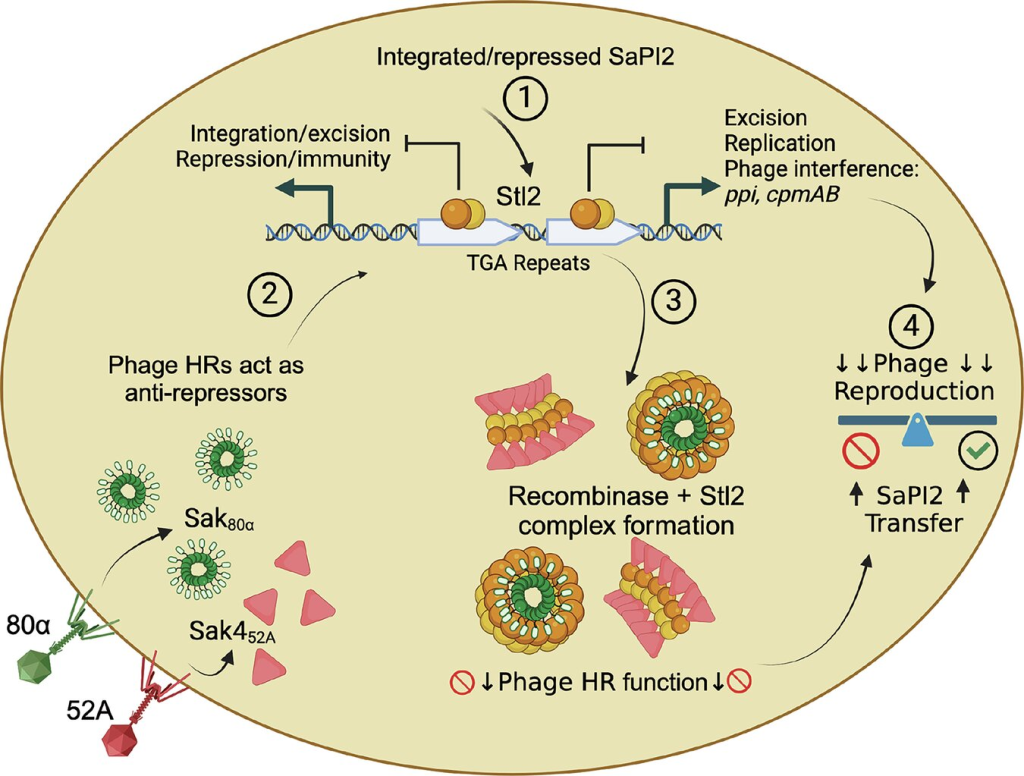
این التهاب بیشازحد میتواند به بیماریهای خودایمنی منجر شود، یعنی حالتی که سیستم ایمنی به اشتباه به بافتهای خود بدن حمله میکند. پژوهشگران بهطور خاص به بیماری لوپوس (SLE یا Systemic Lupus Erythematosus) اشاره کردند، بیماریای که در آن بدن به سلولهای خود آسیب میزند و علائمی مثل خستگی، درد مفاصل و بثورات پوستی ایجاد میکند. آنها با آزمایش خون بیماران مبتلا به لوپوس دریافتند که سطح بالایی از آنتیبادی علیه cA4 در بدنشان وجود دارد، که نشان میدهد این مولکول ممکن است محرکی برای این بیماری باشد.
وضعیت لوپوس در ایران
لوپوس سیستمیک اریتماتوز (SLE)، یک بیماری خودایمنی مزمن، در ایران شیوع قابلتوجهی دارد و یکی از بزرگترین مجموعههای دادههای مربوط به این بیماری در منطقه آسیا و اقیانوسیه در این کشور ثبت شده است. بر اساس مطالعهای که در سال ۲۰۱۰ در مرکز تحقیقات روماتولوژی تهران انجام شد و تا سال ۲۰۰۹ دادهها را پوشش داد، ۲۲۸۰ بیمار مبتلا به لوپوس بررسی شدند. نتایج نشان داد که نسبت زنان به مردان ۹ به ۱ است و میانگین سنی شروع بیماری حدود ۲۴.۴ سال بوده است. شایعترین علائم شامل درگیریهای اسکلتی-عضلانی (۸۳.۲٪)، پوستی (۸۱.۱٪)، کلیوی (۶۵.۴٪) و خونی (۶۶.۴٪) بود. همچنین، آنتیبادیهای ضد هستهای (ANA) در ۸۶.۴٪ و آنتیبادی ضد DNA در ۸۲.۳٪ از بیماران مثبت گزارش شد. این آمار نشان میدهد که لوپوس در ایران الگویی مشابه با کشورهای همسایه از نظر درگیری پوستی و کلیوی دارد، اما درگیریهای خونی و مفصلی آن به کشورهای اروپایی نزدیکتر است، که ممکن است به عوامل ژنتیکی یا محیطی مرتبط باشد.میزان بقا و مرگومیر بیماران لوپوس در ایران نیز مورد توجه قرار گرفته است. مطالعهای در سال ۲۰۱۴ روی بیماران بزرگسال نشان داد که نرخ بقای ۵ ساله ۹۳٪ و ۲۰ ساله ۸۰٪ است، که با روند جهانی قابلقبول همخوانی دارد. با این حال، عواملی مثل درگیری قلبی یا تشنج در زمان تشخیص، بقای بیماران را کاهش میدهد. در کودکان، مطالعهای در سال ۲۰۱۴ روی ۱۲۰ بیمار نشان داد که نرخ مرگومیر ۱۰٪ است و درگیری کبد، قلب و ریه با مرگومیر بالاتر مرتبط است. در مطالعهای دیگر در سال ۲۰۲۳، سن پایینتر، فعالیت شدید بیماری و سابقهی نفریت لوپوس بهعنوان پیشبینهای مستقل شعلهوری شدید بیماری شناسایی شدند. این دادهها نشان میدهد که بیماران ایرانی در مقایسه با برخی کشورهای اروپایی شعلهوری بیشتری دارند، اما کمتر از بیماران آمریکایی. نیاز به نظارت دقیقتر بر بیماران با عوامل خطر و انجام مطالعات چندمرکزی برای درک بهتر الگوی بیماری در ایران احساس میشود.
چگونه این اتفاق میافتد؟
سؤال بزرگ این است: چگونه یک مولکول باکتریایی وارد بدن انسان میشود؟ پاسخ در میکروبیوم ما نهفته است—جامعهی عظیمی از باکتریها که در روده، پوست و دیگر نقاط بدنمان زندگی میکنند. برخی از این باکتریها، مثل گونههای Corynebacterium، میتوانند cA4 را تولید کنند. اگر این مولکولها از طریق نشت روده (Leaky Gut) یا عفونت وارد جریان خون شوند، ممکن است با سیستم ایمنی ما تداخل کنند. این ایده با مطالعات قبلی همخوانی دارد که نشان دادهاند میکروبیوم روده در بیماریهای خودایمنی نقش دارد.
زمینهی علمی: CRISPR و فراتر از آن
CRISPR از دههی ۲۰۰۰ بهعنوان یک ابزار انقلابی در زیستفناوری شناخته شده است، اما نقش طبیعی آن در باکتریها هنوز در حال کشف است. سیستم Cas10 که در این مطالعه بررسی شد، در حدود ۵ درصد از باکتریها یافت میشود و توانایی تولید سیگنالهای شیمیایی مثل cA4 را دارد. این سیگنالها در باکتریها برای هماهنگی دفاع جمعی استفاده میشوند، اما در انسان، به نظر میرسد که به اشتباه سیستم ایمنی را فریب میدهند. این کشف با تحقیقات دیگری که ارتباط بین میکروبها و بیماریهای التهابی را نشان دادهاند، سازگار است.
این پژوهش دو پیامد بزرگ دارد. اول، نشان میدهد که میکروبهای بدن ما چقدر در سلامتیمان تأثیر دارند. ما اغلب باکتریها را بهعنوان دشمن میبینیم، اما آنها همزیستان پیچیدهای هستند که میتوانند هم به ما کمک کنند و هم آسیب برسانند. دوم، این یافته میتواند به توسعهی درمانهای جدید منجر شود. اگر بتوانیم تولید cA4 را در باکتریها مهار کنیم یا واکنش STING را در انسان تنظیم کنیم، شاید راهی برای کاهش شدت بیماریهایی مثل لوپوس پیدا کنیم.
ko-fi.com/itnights
hamibash.com/pnazemi





